Oral corticosteroid reduction and discontinuation in adults with corticosteroid-dependent, severe, uncontrolled asthma treated with tezepelumab (WAYFINDER)
Revisor: Francisco Javier Callejas González, MD, PhD. Servicio de Neumología. Complejo Hospitalario Universitario de Albacete (CHUA).
Palabras clave: Asma grave; tezepelumab; TSLP; corticoides orales; insuficiencia suprarrenal; biológicos, biológicos; ahorro de OCS.
Referencia
Jackson DJ, Lugogo NL, Gurnell M, Heaney LG, Korn S, Brusselle G, Chanez P, del Olmo R, Llanos JP, Keeling N, Sałapa K, Cook B, Parulekar AD, Kostikas K, Fogel R, Martin N, Chandarana SN. Oral corticosteroid reduction and discontinuation in adults with corticosteroid-dependent, severe, uncontrolled asthma treated with tezepelumab (WAYFINDER): a multicentre, single-arm, phase 3b trial. Lancet Respir Med. 2026;14:129–140. doi:10.1016/S2213-2600(25)00359-5.
Tema
Evaluación del efecto ahorrador de corticoides orales (OCS) de tezepelumab en pacientes con asma grave no controlada dependiente de OCS, mediante un protocolo estructurado de reducción progresiva y monitorización sistemática de la función suprarrenal del eje hipotálamo-hipófiso-adrenal.
Resumen
WAYFINDER es un ensayo fase 3b, multicéntrico, abierto y de un solo brazo diseñado específicamente para evaluar el potencial ahorrador de corticoides orales (OCS) de tezepelumab en pacientes con asma grave no controlada dependiente de tratamiento sistémico crónico.
Se incluyeron adultos (18–80 años) en tratamiento con corticoides inhalados a dosis altas asociados a LABA y que recibían una dosis estable de prednisona/prednisolona entre 5 y 40 mg/día durante al menos 3 meses previos. Todos debían haber presentado al menos una exacerbación en el año anterior. El estudio reclutó 298 pacientes tratados, con una dosis basal media de 10,8 mg/día. Aproximadamente el 42% presentaba eosinofilia ≥ 300 células/µL, mientras que un 29% tenía < 150 células/µL, reflejando una cohorte con fenotipos inflamatorios heterogéneos.
El diseño (figura 1) contempló una fase de inducción inicial de 4 semanas con mantenimiento de la dosis basal de OCS, seguida de una fase de reducción progresiva durante 48 semanas. Tezepelumab se administró a dosis de 210 mg subcutáneos cada 4 semanas durante un total de 52 semanas.
Figura 1. Diseño del estudio WAYFINDER (A) y protocolos de reducción progresiva de OCS (B) y evaluación de la función suprarrenal (C).
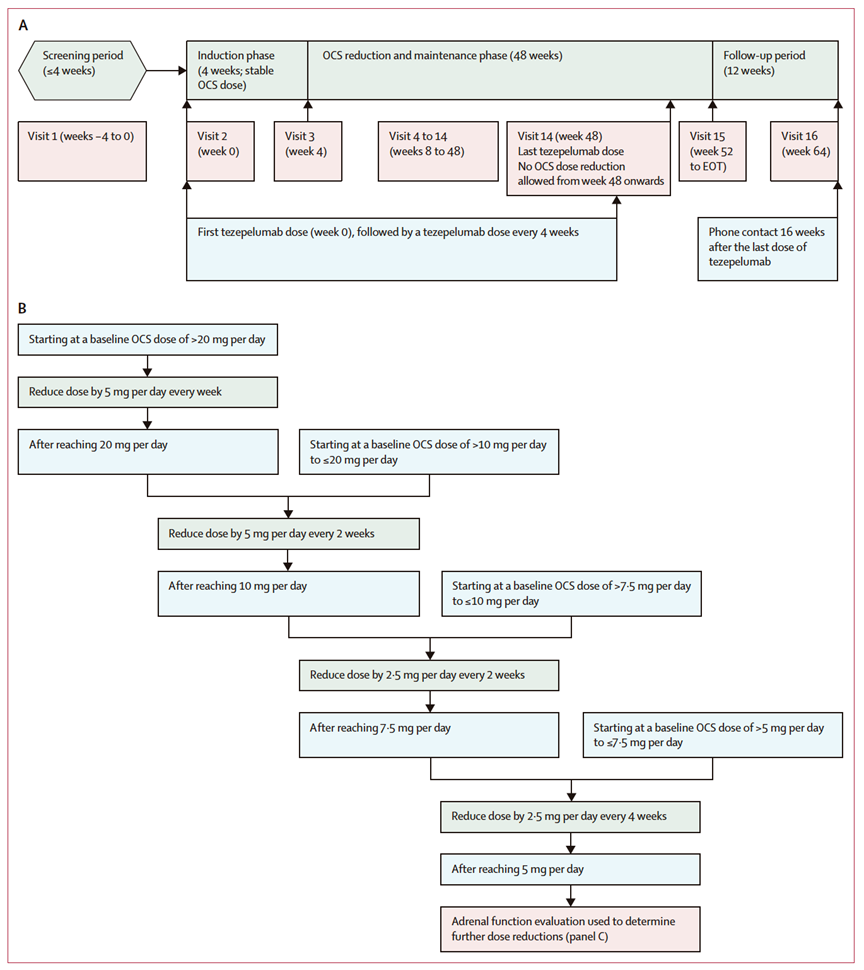
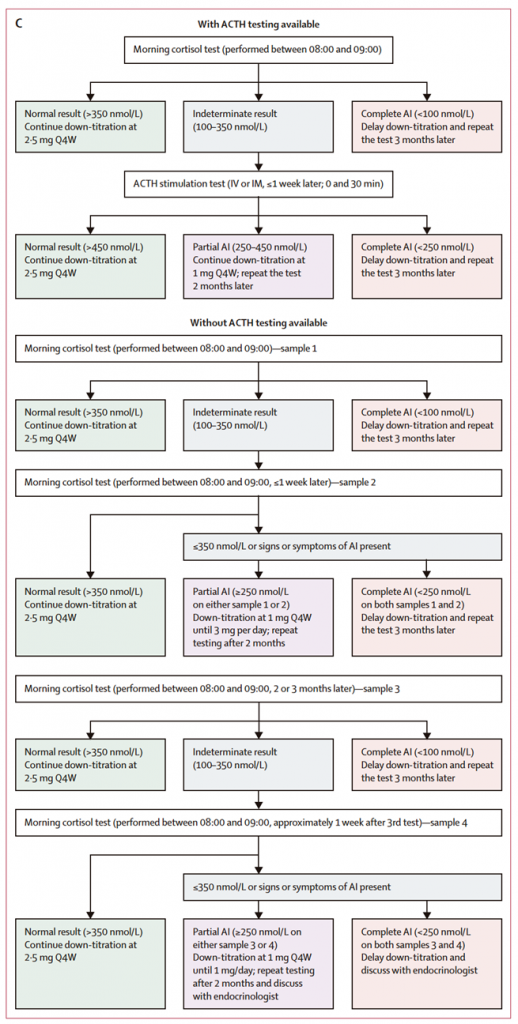
(B) Durante la fase de reducción y mantenimiento de OCS, la dosis de corticoides orales se disminuyó progresivamente, siempre que se mantuviera el control del asma, hasta alcanzar una dosis de 5 mg/día de prednisona o prednisolona. (C) La evaluación de la función suprarrenal se realizó mediante determinación de cortisol sérico matutino en aquellos participantes que se encontraban en una dosis estable de OCS de 5 mg/día durante al menos 4 semanas; la reducción posterior desde 5 mg/día se llevó a cabo en función del estado suprarrenal. Si la función suprarrenal resultaba indeterminada en la primera determinación, se realizaba una segunda prueba (test de estimulación con ACTH, si estaba disponible, o determinaciones repetidas de cortisol matutino) para confirmar el estado suprarrenal y decidir si continuar con la reducción de OCS. Se emplearon rangos alternativos de cortisol en participantes que tomaban anticonceptivos con estrógenos.
Abreviaturas: ACTH = hormona adrenocorticótropa; AI = insuficiencia suprarrenal, EOT = fin de tratamiento; IM = intramuscular, IV = intravenoso; OCS = corticoide oral, Q4W = cada 4 semanas.
El descenso de OCS siguió un protocolo personalizado en función de la dosis inicial: reducciones más rápidas desde dosis altas y más conservadoras al aproximarse a 5 mg/día. Una vez alcanzada dicha dosis, se evaluó sistemáticamente la integridad del eje hipotálamo-hipófiso-adrenal mediante cortisol sérico matutino y, cuando estaba disponible, test de estimulación con ACTH. Las reducciones posteriores dependían tanto del control clínico del asma como del estado funcional suprarrenal, permitiendo una titulación individualizada y segura.
Los co-objetivos primarios fueron la proporción de pacientes que alcanzaban ≤ 5 mg/día sin pérdida de control y la proporción que lograba la retirada completa de OCS, evaluados en semanas 28 y 52. A la semana 28, el 88,9% habían reducido a ≤ 5 mg/día y el 32,2% habían suspendido completamente los OCS; a la semana 52, el 89,9% alcanzaron ≤ 5 mg/día sin deterioro clínico y el 50,3% lograron la suspensión completa del OCS (figura 2). El 81,9% consiguió reducciones ≥ 50% respecto a la dosis basal, con una reducción media del 72%, siendo los resultados consistentes en subgrupos definidos por eosinofilia, FeNO y estado alérgico (figura 3).
Figura 2. Proporción de pacientes que alcanzan ≤5 mg/día o retirada completa de OCS.
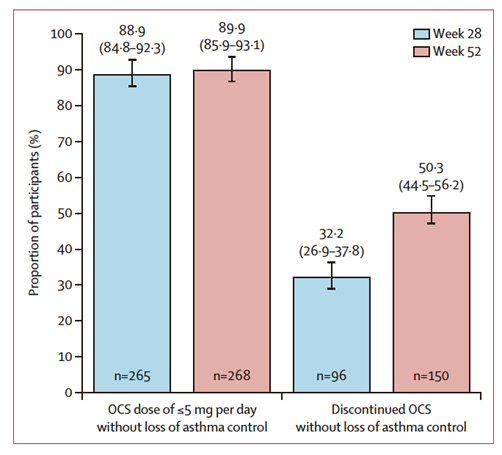
Figura 3. Resultados por subgrupos según eosinofilia basal y FeNO.
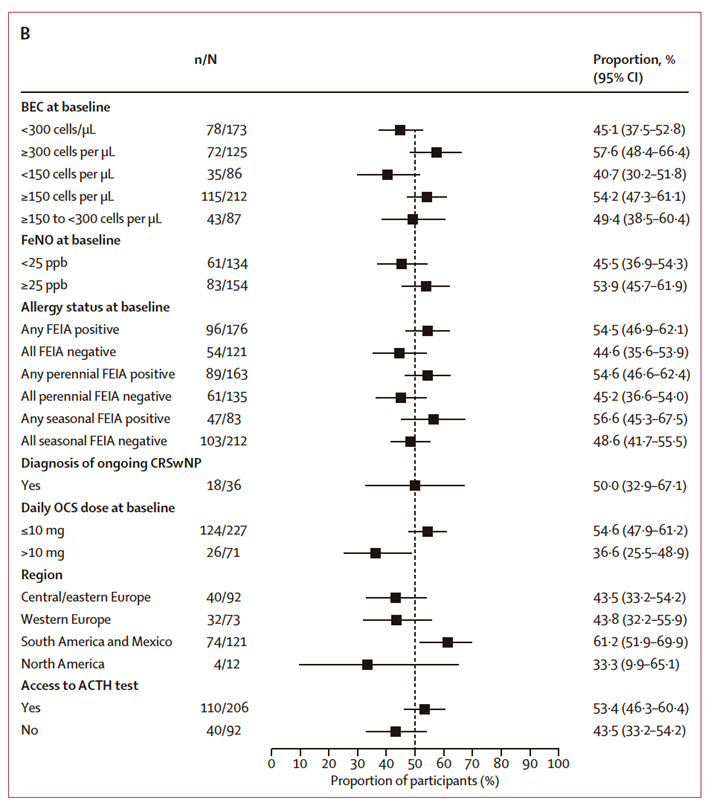
La reducción de OCS fue consistente tanto en pacientes con eosinofilia ≥ 300 células/µL como en aquellos con valores < 150 células/µL, confirmando la eficacia transversal del bloqueo de TSLP, independientemente del fenotipo inflamatorio clásico T2.
Más de dos tercios de los pacientes permanecieron libres de exacerbaciones, con estabilidad funcional (FEV1) y mejoría sostenida del control sintomático y calidad de vida, lo que consolida el efecto clínico global del tratamiento, sin, además, identificarse nuevas señales relevantes de seguridad.
Conclusiones
Tezepelumab permite una desescalada eficaz y segura de corticoides orales en asma grave dependiente de OCS. Así, la mitad de los pacientes lograron la retirada completa en un año y casi el 90% alcanzó dosis fisiológicas, con mantenimiento del control clínico.
Comentario
WAYFINDER aporta evidencia clínicamente muy relevante en un escenario de alta carga asistencial, el manejo del paciente con asma grave dependiente de corticoides sistémicos.
A diferencia del estudio SOURCE, cuyo diseño controlado limitó la interpretación del efecto ahorrador, WAYFINDER incorpora un protocolo estructurado de descenso rápido de OCS con evaluación endocrinológica activa, lo que lo aproxima mucho más a la práctica clínica real y ofrece una guía aplicable en consultas monográficas de asma grave.
Es especialmente relevante que el efecto sea consistente independientemente del nivel basal de eosinofilia o FeNO, reforzando la posición de tezepelumab como biológico de espectro amplio, útil en fenotipos T2 altos y bajos.
En conjunto, WAYFINDER consolida el cambio de paradigma hacia la eliminación progresiva del OCS crónico como objetivo prioritario en el manejo del asma grave en la era de los biológicos.
Bibliografía
- Jackson DJ, Lugogo NL, Gurnell M, Heaney LG, Korn S, Brusselle G, Chanez P, del Olmo R, Llanos JP, Keeling N, Sałapa K, Cook B, Parulekar AD, Kostikas K, Fogel R, Martin N, Chandarana SN. Oral corticosteroid reduction and discontinuation in adults with corticosteroid-dependent, severe, uncontrolled asthma treated with tezepelumab (WAYFINDER): a multicentre, single-arm, phase 3b trial. Lancet Respir Med. 2026;14:129–140. doi:10.1016/S2213-2600(25)00359-5.
- Global Initiative for Asthma. Global strategy for asthma management and prevention 2025. https://ginasthma.org/2025-gina-main-report/ (accessed Feb 28, 2026).
- Volmer T, Effenberger T, Trautner C, Buhl R. Consequences of longterm oral corticosteroid therapy and its side-effects in severe asthma in adults: a focused review of the impact data in the literature. Eur Respir J 2018; 52: 52.
- Gurnell M, Heaney LG, Price D, Menzies-Gow A. Long-term corticosteroid use, adrenal insufficiency and the need for steroidsparing treatment in adult severe asthma. J Intern Med 2021; 290: 240–56.
- Gauvreau GM, O’Byrne PM, Boulet LP, et al. Effects of an anti-TSLP antibody on allergen-induced asthmatic responses. N Engl J Med 2014; 370: 2102–10.
- Menzies-Gow A, Corren J, Bourdin A, et al. Tezepelumab in adults and adolescents with severe, uncontrolled asthma. N Engl J Med 2021; 384: 1800–09.
- Bel EH, Wenzel SE, Thompson PJ, et al, and the SIRIUS Investigators. Oral glucocorticoid-sparing effect of mepolizumab in eosinophilic asthma. N Engl J Med 2014; 371: 1189–97.
- Nair P, Wenzel S, Rabe KF, et al, and the ZONDA Trial Investigators. Oral glucocorticoid-sparing effect of benralizumab in severe asthma. N Engl J Med 2017; 376: 2448–58.
- Rabe KF, Nair P, Brusselle G, et al. Efficacy and safety of dupilumab in glucocorticoid-dependent severe asthma. N Engl J Med 2018; 378: 2475–85.
- Menzies-Gow A, Wechsler ME, Brightling CE, et al, and the DESTINATION study investigators. Long-term safety and efficacy of tezepelumab in people with severe, uncontrolled asthma (DESTINATION): a randomised, placebo-controlled extension study. Lancet Respir Med 2023; 11: 425–38.
- Wechsler ME, Menzies-Gow A, Brightling CE, et al, and the SOURCE study group. Evaluation of the oral corticosteroid-sparing effect of tezepelumab in adults with oral corticosteroid-dependent asthma (SOURCE): a randomised, placebo-controlled, phase 3 study. Lancet Respir Med 2022; 10: 650–60.
- Wechsler ME, Stolz D, Lugogo NL, et al. Oral and inhaled corticosteroid dose reductions with tezepelumab versus placebo in patients with severe, uncontrolled asthma from DESTINATION. J Allergy Clin Immunol Pract 2024; 12: 3128–3131.e2.
- Chen W, Tran TN, Sadatsafavi M, et al. Impact of initiating biologics in patients with severe asthma on long-term oral corticosteroids or frequent rescue steroids (GLITTER): data from the International Severe Asthma Registry. J Allergy Clin Immunol Pract 2023; 11: 2732–47.
- Carr TF, Moore WC, Kraft M, et al. Efficacy of tezepelumab in patients with severe, uncontrolled asthma across multiple clinically relevant subgroups in the NAVIGATOR study. Adv Ther 2024; 41: 2978–90.