Revisora: Dra. Tamara Hermida Valverde, Unidad de Asma, Servicio de Neumología Hospital Universitario Central de Asturias.
Palabras clave: Asma, Rasgos Tratables, Tratamiento.
Autores: Kanabar SS, Pavord ID, Hinks TSC
Referencia: Kanabar SS, Pavord ID, Hinks TSC. Treatable traits and treatment options in asthma. Respir Med. 2026 Apr;254:108736. doi: 10.1016/j.rmed.2026.108736. Epub 2026 Feb 27. PMID: 41763276.
Resumen:
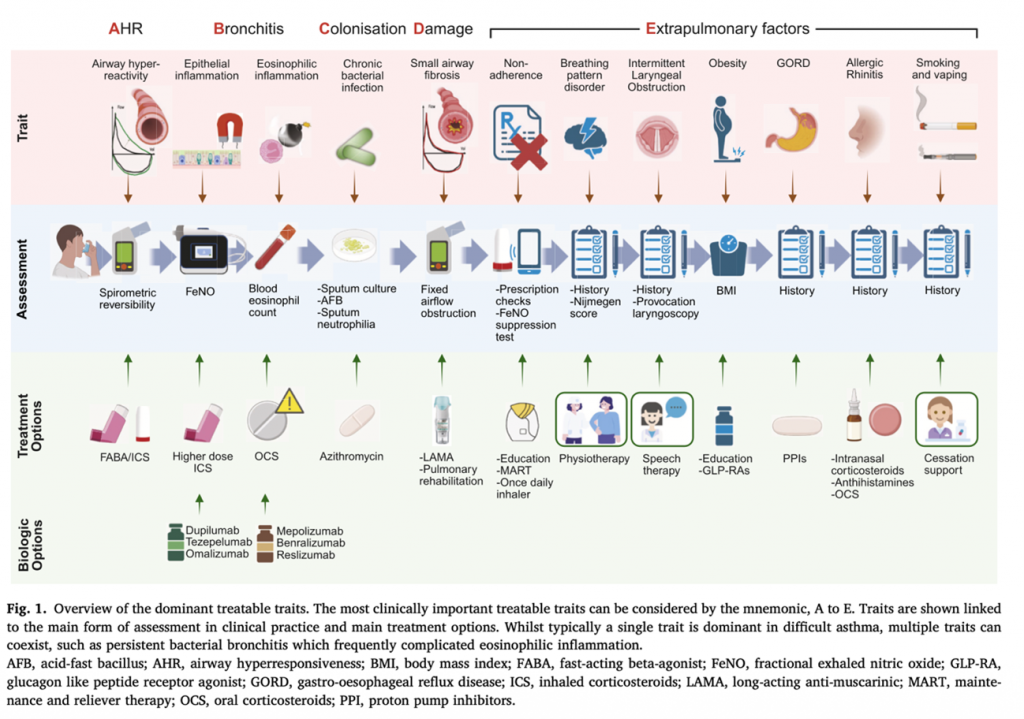
En la era de la medicina personalizada, el enfoque del manejo del asma ha evolucionado de considerar la enfermedad como un proceso lineal y homogéneo a verla como un conjunto de procesos biológicos complejos con interrelaciones diversas1-4. El modelo tradicional, donde la exposición a alérgenos induce una inflamación eosinofílica simple, ha demostrado ser insuficiente para explicar la heterogeneidad clínica observada en pacientes con asma difícil y grave. Por ello, se propone el paradigma de los «rasgos tratables», que consiste en dividir las enfermedades de las vías respiratorias en características específicas que sean tanto identificables y medibles, como modificables mediante intervenciones terapéuticas 3-7. Este enfoque permite una estratificación precisa de los pacientes y el uso eficaz de terapias biológicas dirigidas. El estudio estructura estos rasgos mediante la mnemotecnia «A a E» para facilitar su evaluación en la práctica clínica 8-11.
A – Hiperreactividad de las vías respiratorias
La broncodilatación farmacológica ha sido el pilar del tratamiento del asma durante más de un siglo 12. Actualmente, se prefieren los inhaladores de combinación de dosis fija que contienen LABA/ICS (beta-agonista de acción rápida y corticoide inhalado, como formoterol/budesonida) como primera línea de tratamiento. La combinación de un corticoide inhalado (ICS) en cada dosis ayuda a minimizar la falta de adherencia. Existe evidencia sólida de que el uso de estos inhaladores guiado por los síntomas es eficaz para reducir las exacerbaciones y hospitalizaciones en comparación con el uso exclusivo de SABA (beta-agonistas de acción corta). En el asma moderada, el régimen de mantenimiento y rescate (MART) ha demostrado ser superior a los regímenes de dosis fija tradicionales13-16. Una alternativa para mejorar la adherencia es el uso de combinaciones de acción ultraprolongada de una sola dosis diaria, como fluticasona furoato con vilanterol17-18.
B – Bronquitis
El asma se caracteriza predominantemente por una inflamación de tipo 2 (T2) impulsada por citoquinas como IL-4, IL-5 e IL-13, y mediada por alarminas epiteliales como TSLP e IL-33. El estudio propone un marco conceptual de dos compartimentos: el «imán» y la «bomba» 19,20.
– El «Imán» (FeNO): El óxido nítrico exhalado (FeNO) es un biomarcador que refleja la inflamación de la mucosa de las vías respiratorias y la atracción quimiotáctica de los eosinófilos hacia ellas. Los pacientes con FeNO elevado suelen responder bien a los ICS y a biológicos dirigidos a la vía de la IL-4/13 (como dupilumab) o a las alarminas epiteliales (como tezepelumab) 21,22.
– La «Bomba» (Eosinófilos en sangre): El recuento de eosinófilos en sangre periférica correlaciona con la IL-5 sistémica y representa el pool de células efectoras disponibles. Estos pacientes responden mejor a los corticoides sistémicos o a biológicos dirigidos al eje IL-5/IL-5R (como mepolizumab, benralizumab o reslizumab) 23-26.
C – Colonización bacteriana
La infección respiratoria crónica de las vías respiratorias inferiores es un rasgo tratable común en el asma grave, identificándose bacterias como Haemophilus influenzae, Moraxella catarrhalis o Streptococcus pneumoniae en el 23-34% de los casos. Esta carga bacteriana suele asociarse con neutrofilia en el esputo y resistencia a los corticoides. Se ha demostrado que el tratamiento a largo plazo con azitromicina en dosis bajas (500 mg tres veces por semana) reduce significativamente la proporción de pacientes que experimentan exacerbaciones y mejora su calidad de vida. Antes de iniciar este tratamiento, es necesario realizar un cribado mediante electrocardiograma para excluir la prolongación del intervalo QT y descartar infecciones por micobacterias no tuberculosas 27-29.
D – Daño
Se refiere a la obstrucción fija del flujo aéreo debida a la remodelación de las vías respiratorias. En estos pacientes, la adición de un antagonista muscarínico de acción prolongada (LAMA) o el uso de triple terapia (LABA/LAMA/ICS) proporciona mejoras modestas en la función pulmonar y puede reducir las exacerbaciones graves hasta en un 17% 30.
E – Factores extrapulmonares
– Falta de adherencia: Identificada en el 39-52% de los pacientes con asma grave. El uso de dispositivos de monitorización electrónica (EMD) y la simplificación de los regímenes a una dosis diaria han demostrado mejorar la concordancia 1.
– Trastornos del patrón respiratorio: Presentes en el 47% de los pacientes con asma difícil, mimetizando a menudo los síntomas del asma. Suelen coexistir con ansiedad y depresión 31.
– Obstrucción laríngea inducible (OLI): Afecta al 25% de los pacientes y se caracteriza por una aducción anormal de las cuerdas vocales. El diagnóstico se confirma mediante laringoscopia y el tratamiento se basa en técnicas de logopedia 32.
– Obesidad: Es un factor determinante en la discapacidad por asma. El uso de agonistas del receptor de GLP-1 (GLP-1RA) es una vía prometedora para mejorar el control del asma en pacientes obesos al reducir la inflamación sistémica 33.
– Tabaquismo y vapeo: El humo del tabaco aumenta los eventos adversos, y el uso de cigarrillos electrónicos interfiere con la homeostasis inmune normal de las vías respiratorias 1.
Conclusión: El enfoque de los rasgos tratables permite un diagnóstico temprano de comorbilidades y el uso de biológicos que reducen la necesidad de corticoides sistémicos. El futuro del tratamiento incluye biológicos de acción ultraprolongada como el depemokimab (anti-IL-5 de administración semestral) y nuevas moléculas orales como el rilzabrutinib (inhibidor de la BTK), que prometen mejoras rápidas en los síntomas diarios al bloquear la activación de mastocitos y basófilos 34,.
Comentario:
Este trabajo consolida el paradigma de los «rasgos tratables», permitiendo una transición real hacia la medicina de precisión en el asma grave. Parece clave dividir la complejidad de la enfermedad mediante la mnemotecnia «A a E», lo que facilita una evaluación diagnóstica y terapéutica estructurada en la práctica clínica.
Es particularmente valioso el modelo de «imán y bomba», que distingue la inflamación mucosa (FeNO) de la sistémica (eosinófilos en sangre), optimizando la elección de terapias biológicas dirigidas. Además, el enfoque global al abordar la obesidad como principal factor de discapacidad y el uso de azitromicina para la infección bronquial crónica demuestra una visión integral que va más allá de la vía aérea.
Sin embargo, el estudio evidencia limitaciones en la identificación de rasgos como los trastornos del patrón respiratorio o la obstrucción laríngea inducible (OLI), que siguen siendo difíciles de diagnosticar de forma objetiva por la falta de definiciones consensuadas y herramientas específicas.
En conclusión, este planteamiento de modelo integral puede suponer mejoras a nivel clínico y de control de riesgos futuros (exacerbaciones, toma de corticoides sistémicos, etc). Representa una hoja de ruta esencial para una atención personalizada, aunque el diagnóstico de ciertos rasgos extrapulmonares aún requiere matizaciones y estudio.
Bibliografía:
- Global Initiative for Asthma. Global strategy for asthma management and prevention. 2023.
- Anderson GP. Endotyping asthma: new insights into key pathogenic mechanisms in a complex, heterogeneous disease. Lancet. 2008;372(9643):1107-1119.
- Hinks TS, Zhou X, Staples KJ, Dimitrov BD, Manta A, Petrossian T, et al. Innate and adaptive T cells in asthmatic patients: relationship to severity and disease mechanisms. J Allergy Clin Immunol. 2015;136(2):323-333.
- Hinks TSC, Brown T, Lau LCK, Rupani H, Barber C, Elliott S, et al. Multidimensional endotyping in patients with severe asthma reveals inflammatory heterogeneity in matrix metalloproteinases and chitinase 3-like protein 1. J Allergy Clin Immunol. 2016;138(1):61-75.
- Haldar P, Pavord ID, Shaw DE, Berry MA, Thomas M, Brightling CE, et al. Cluster analysis and clinical asthma phenotypes. Am J Respir Crit Care Med. 2008;178(3):218-224.
- Kuo CS, Pavlidis S, Loza M, Baribaud F, Rowe A, Pandis I, et al. A transcriptome-driven analysis of epithelial brushings and bronchial biopsies to define asthma phenotypes in U-BIOPRED. Am J Respir Crit Care Med. 2017;195(4):443-455.
- Pavord ID, Beasley R, Agusti A, Anderson GP, Bel E, Brusselle G, et al. After asthma: redefining airways diseases. Lancet. 2018;391(10118):350-400.
- Haldar P, Brightling CE, Hargadon B, Gupta S, Monteiro W, Sousa A, et al. Mepolizumab and exacerbations of refractory eosinophilic asthma. N Engl J Med. 2009;360(10):973-984.
- Pavord ID, Korn S, Howarth P, Bleecker ER, Buhl R, Keene ON, et al. Mepolizumab for severe eosinophilic asthma (DREAM): a multicentre, double-blind, placebo-controlled trial. Lancet. 2012;380(9842):651-659.
- Flood-Page P, Swenson C, Faiferman I, Matthews J, Williams M, Brannick L, et al. A study to evaluate safety and efficacy of mepolizumab in patients with moderate persistent asthma. Am J Respir Crit Care Med. 2007;176(11):1062-1071.
- Leckie MJ, ten Brinke A, Khan J, Diamant Z, O’Connor BJ, Walls CM, et al. Effects of an interleukin-5 blocking monoclonal antibody on eosinophils, airway hyper-responsiveness, and the late asthmatic response. Lancet. 2000;356(9248):2144-2148.
- Rabe KF, Atienza T, Magyar P, Larsson P, Jorup C, Lalloo UG. Effect of budesonide in combination with formoterol for reliever therapy in asthma exacerbations: a randomised controlled, double-blind study. Lancet. 2006;368(9537):744-753.
- Busse WW, O’Byrne PM, Bleecker ER, Lotvall J, Woodcock A, Andersen L, et al. Safety and tolerability of the novel inhaled corticosteroid fluticasone furoate in combination with the beta2 agonist vilanterol administered once daily for 52 weeks in patients aged >=12 years with asthma: a randomised trial. Thorax. 2013;68(6):513-520.
- Devillier P, Humbert M, Boye A, Zachgo W, Jacques L, Nunn C, et al. Efficacy and safety of once-daily fluticasone furoate/vilanterol (FF/VI) versus twice-daily inhaled corticosteroids/long-acting beta agonists. Respir Med. 2018;141:111-120.
- Lambrecht BN, Hammad H, Fahy JV. The cytokines of asthma. Immunity. 2019;50(4):975-991.
- Marchi E, Hinks TSC, Richardson M, Khalfaoui L, Symon FA, Rajasekar P, et al. The effects of inhaled corticosteroids on healthy airways. Allergy. 2024;79(7):1831-1843.
- Syed YY. Fluticasone furoate/vilanterol: a review of its use in patients with asthma. Drugs. 2015;75(4):407-418.
- Svedsater H, Jones R, Bosanquet N, Jacques L, Lay-Flurrie J, Leather DA, et al. Patient-reported outcomes with initiation of fluticasone furoate/vilanterol versus continuing usual care in the Asthma Salford Lung Study. Respir Med. 2018;141:198-206.
- Couillard S, Jackson DJ, Wechsler ME, Pavord ID. Workup of severe asthma. Chest. 2021;160(6):2019-2029.
- Couillard S, Shrimanker R, Chaudhuri R, Mansur AH, McGarvey LP, Heaney LG, et al. Fractional exhaled nitric oxide nonsuppression identifies corticosteroid-resistant type 2 signaling in severe asthma. Am J Respir Crit Care Med. 2021;204(6):731-734.
- Shrimanker R, Keene O, Hynes G, Wenzel S, Yancey S, Pavord ID. Prognostic and predictive value of blood eosinophil count, fractional exhaled nitric oxide, and their combination in severe asthma: a post hoc analysis. Am J Respir Crit Care Med. 2019;200(10):1308-1312.
- Menzies-Gow A, Corren J, Bourdin A, Chupp G, Israel E, Wechsler ME, et al. Tezepelumab in adults and adolescents with severe, uncontrolled asthma. N Engl J Med. 2021;384(19):1800-1809.
- Ortega HG, Yancey SW, Mayer B, Gunsoy NB, Keene ON, Bleecker ER, et al. Severe eosinophilic asthma treated with mepolizumab stratified by baseline eosinophil thresholds: a secondary analysis of the DREAM and MENSA studies. Lancet Respir Med. 2016;4(7):549-556.
- Ortega HG, Liu MC, Pavord ID, Brusselle GG, FitzGerald JM, Chetta A, et al. Mepolizumab treatment in patients with severe eosinophilic asthma. N Engl J Med. 2014;371(13):1198-1207.
- Nair P, Wenzel S, Rabe KF, Bourdin A, Lugogo NL, Kuna P, et al. Oral glucocorticoid-sparing effect of benralizumab in severe asthma. N Engl J Med. 2017;376(25):2448-2458.
- Castro M, Zangrilli J, Wechsler ME, Bateman ED, Brusselle GG, Bardin P, et al. Reslizumab for inadequately controlled asthma with elevated blood eosinophil counts: results from two multicentre, parallel-group, double-blind, randomised, placebo-controlled, phase 3 trials. Lancet Respir Med. 2015;3(5):355-366.
- Jabeen MF, Sanderson ND, Foster D, Crook DW, Cane JL, Borg C, et al. Identifying bacterial airways infection in stable severe asthma using Oxford nanopore sequencing technologies. Microbiol Spectr. 2022;10(2):e0227921.
- Ahearn CP, Gallo MC, Murphy TF. Insights on persistent airway infection by non-typeable Haemophilus influenzae in chronic obstructive pulmonary disease. Pathog Dis. 2017;75(4).
- Serisier DJ. Risks of population antimicrobial resistance associated with chronic macrolide use for inflammatory airway diseases. Lancet Respir Med. 2013;1(3):262-274.
- Kim LHY, Saleh C, Whalen-Browne A, O’Byrne PM, Chu DK. Triple vs dual inhaler therapy and asthma outcomes in moderate to severe asthma: a systematic review and meta-analysis. JAMA. 2021;325(24):2466-2477.
- Denton E, Bondarenko J, Tay T, Lee J, Radhakrishna N, Hore-Lacy F, et al. Factors associated with dysfunctional breathing in patients with difficult-to-treat asthma. J Allergy Clin Immunol Pract. 2019;7(5):1471-1476.
- Weinberger M. VCD and ILO are not synonymous. J Allergy Clin Immunol. 2023;152(6):1687-1688.
- Foer D, Beeler PE, Cui J, Karlson EW, Bates DW, Cahill KN. Asthma exacerbations in patients with type 2 diabetes and asthma on glucagon-like peptide-1 receptor agonists. Am J Respir Crit Care Med. 2021;203(7):831-840.
- Jackson DJ, Wechsler ME, Bernstein D, Korn S, Pfeffer PE, Chen R, et al. Twice-yearly depemokimab in severe asthma with an eosinophilic phenotype. N Engl J Med. 2024;391(24):2337-2349.
- Pavord ID, Laidlaw TM, Busse W, Maspero J, Liu T, Gereige J, et al. Late Breaking Abstract – Efficacy of high- and low-dose rilzabrutinib from a phase 2 study. Eur Respir J. 2024;64(suppl 68):OA2774.