Assessment of the long-term safety of mepolizumab and durability of clinical response in patients with severe eosinophilic asthma.
Artículo seleccionado:
Khatri S, Moore W, Gibson PG, Leigh R, Bourdin A, Maspero J, Barros M, Buhl R, Howarth P, Albers FC, Bradford ES, Gilson M, Price RG, Yancey SW, Ortega H.
J Allergy Clin Immunol. 2019 May;143(5):1742-1751.e7.
Revisor:
Dra. Elena Curto Sánchez
Unidad de Asma, Servicio de Neumología y Alergia. Hospital de la Santa Creu i de Sant Pau. Barcelona.
Palabras clave: asma grave, eosinofilia, mepolizumab, anticuerpos monoclonales, anti IL-5, seguridad, eficacia
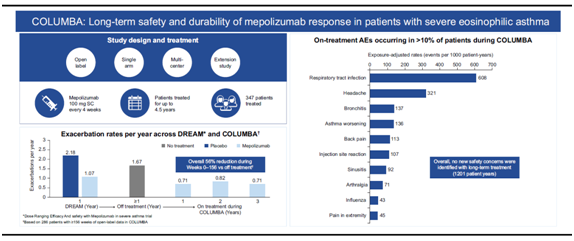
El mepolizumab es un anticuerpo monoclonal humanizado dirigido contra la IL5, disponible desde hace más de un año para el tratamiento del asma eosinofílica grave. Numerosos ensayos clínicos han demostrado su seguridad y eficacia durante un año, pero este es el estudio que lo evalúa durante el periodo más prolongado. Es una extensión abierta de los pacientes con asma eosinofílica grave que previamente hubieran sido participantes del estudio DREAM, con un periodo medio de descanso del fármaco de 12 meses y un seguimiento total de entre 3,5 y 4,5 años.
Se incluyó un total de 347 pacientes, si bien se descartaron los que hubieran presentado efectos adversos graves durante el estudio DREAM. En la mayoría de los pacientes se registraron efectos adversos (94%), pero únicamente un 28% fueros atribuidos al fármaco por el investigador. Los más frecuentes fueron la infección de vías respiratorias, la cefalea y el empeoramiento del asma. La incidencia de efectos adversos graves fue del 23%, y se registraron seis muertes, pero ninguna relacionada con la administración de mepolizumab. Se reportaron ocho casos de herpes zoster.
Los datos de eficacia confirman los resultados obtenidos previamente: hubo una reducción de las exacerbaciones en un 61% respecto al periodo sin tratamiento que los pacientes pasaron entre el estudio DREAM y el COLUMBA. El control, medido por ACQ-5, mejoró de forma significativa durante todo el estudio (0,47 puntos de media) y la función pulmonar experimentó una mejoría inicial para volver a sus niveles previos a lo largo del registro. Se observó un descenso del 78% en el nivel de eosinófilos mantenido a partir de la cuarta semana. Se realizó un análisis post hoc dividiendo a los pacientes según el debut del asma (en antes y después de los 33 años), y no hubo diferencia a nivel de eficacia ni de seguridad. Se detectaron anticuerpos antifármaco en un 8% de los pacientes que no se relacionaron con una peor respuesta clínica ni con mayor incidencia de reacciones de hipersensibilidad.
Comentario
Este estudio aporta los resultados de seguridad y eficacia a más largo plazo disponibles para un anticuerpo monoclonal anti IL-5, y en concreto para el mepolizumab, y demuestra que es un fármaco seguro y especialmente útil en la prevención de exacerbaciones pero con escaso efecto sobre la función pulmonar incluso tras un periodo largo de administración. Tras más de un año en el mercado, el mepolizumab ya cuenta con multitud de estudios que apoyan su eficacia, su seguridad, su papel como reductor de exacerbaciones y ahorrador de corticoides, incluso con resultados en la vida real. Además, este estudio aporta datos respecto a la eficacia y la seguridad de la reexposición, pues evalúa pacientes que ya habían recibido el fármaco previamente y tuvieron un periodo de descanso del mismo. Tras volver a iniciar la administración, los resultados de tolerancia y eficacia se mantienen, y no hubo un aumento significativo de la producción de anticuerpos contra el fármaco. Al evaluar la respuesta a largo plazo, se ha observado que tras una mejoría inicial los valores de FEV1 vuelven a los basales hacia la semana 200, dato que se desconocía previamente y que los autores relacionan con la gravedad de la población de estudio, el curso natural de la enfermedad y una posible reducción en la medicación de mantenimiento de los pacientes.
Como limitación principal, existe un sesgo de selección, puesto que los pacientes con efectos adversos graves o reacciones de hipersensibilidad en el estudio DREAM no fueron incluidos en este estudio, por lo que los datos disponibles son de pacientes con buena tolerancia previa demostrada. Sin embargo esta situación probablemente ocurra también en práctica clínica diaria, por lo que se puede confirmar que una buena tolerancia inicial asegura un buen perfil de seguridad a largo plazo.